1. La solution a-t-elle démontré un impact clinique mesurable sur la mortalité et les hospitalisations ?
Les recommandations ESC 2021 précisent que la télésurveillance peut être recommandée lorsqu’elle améliore les résultats cliniques des patients insuffisants cardiaques (McDonagh TA et al., European Heart Journal, 2021;42:3599-3726). L’étude nationale TELESAT-HF, publiée dans le European Journal of Heart Failure en 2024 (Girerd N. et al., doi:10.1002/ejhf.3563), rapporte :
-
–36 % de mortalité toutes causes,
-
–48 % chez les patients les plus sévères,
-
–17 % d’hospitalisations en urgence pour décompensation.

L’étude TELESAT-HF visait à comprendre l’impact de la télésurveillance sur les patients atteints d’insuffisance cardiaque en vie réelle. Grâce à son ampleur inégalée, TELESAT-HF offre des perspectives uniques sur l’efficacité et les bénéfices de la télésurveillance dans le traitement de l’insuffisance cardiaque
Ces résultats ont été obtenus en conditions réelles à l’échelle nationale. Dans un appel d’offres télésurveillance insuffisance cardiaque, il est donc pertinent d’exiger :
-
des publications scientifiques indexées,
-
des données en vie réelle,
-
des indicateurs cliniquement significatifs (mortalité, hospitalisations).
La preuve clinique publiée constitue un critère objectif de différenciation.
2. La solution respecte-t-elle strictement le cadre réglementaire du droit commun ?
L’Arrêté du 22 juin 2023 (JO du 24 juin 2023) et le cahier des charges de la HAS définissent précisément les exigences applicables aux dispositifs de télésurveillance. La section C du référentiel précise notamment :
-
la transmission obligatoire du poids,
-
l’intégration d’un questionnaire relatif aux symptômes et signes précurseurs de décompensation,
-
l’émission d’alertes non désactivables,
-
la traçabilité des transmissions.
L’Assurance Maladie rappelle :
« Le repérage des signaux d’alerte constitue l’un des principaux leviers d’actions pour une prise en charge optimale. »
(Mémo insuffisance cardiaque – Assurance Maladie, 24 mars 2023)
Il est donc essentiel d’examiner :
-
le nombre de questions symptomatiques obligatoires,
-
leur adéquation aux signes cliniques décrits (essoufflement, œdèmes, fatigue, prise de poids, etc.),
-
la fréquence configurable des transmissions.
Le référentiel mentionne également l’existence d’une fonction de collecte de questionnaires validés de qualité de vie. Des outils tels que l’EQ-5D-5L ou le Minnesota Living with Heart Failure Questionnaire peuvent répondre à cette exigence.
3. Le marquage CE correspond-il à une revendication clinique documentée ?
Dans le cadre du règlement (UE) 2017/745 relatif aux dispositifs médicaux (MDR), les solutions de télésurveillance destinées à la prise en charge clinique des patients insuffisants cardiaques doivent être marquées CE, généralement en classe IIa. Cependant, la classe CE, à elle seule, ne préjuge pas du niveau de preuve clinique associé. Un dispositif CE IIa peut reposer :
-
soit sur une revendication essentiellement technique (sécurité, fonctionnement, gestion des données) ;
-
soit sur une revendication de performance clinique, impliquant que le fabricant démontre l’effet revendiqué sur des critères cliniques pertinents.
La différence est déterminante.
Dans un appel d’offres télésurveillance insuffisance cardiaque, il ne suffit donc pas de vérifier la présence du marquage CE IIa. Il convient également de demander :
-
quelle est la revendication clinique exacte portée par le dispositif ;
-
quels sont les critères cliniques revendiqués (réduction d’hospitalisations, amélioration de la qualité de vie, réduction de mortalité…) ;
-
quelles données cliniques ont été fournies à l’organisme notifié pour justifier cette revendication ;
-
si ces données ont fait l’objet de publications scientifiques indépendantes.
À l’approche des échéances réglementaires et des réévaluations prévues, cette distinction prend une importance particulière : deux dispositifs de même classe réglementaire peuvent présenter des niveaux de preuve très différents.
Enfin, la présence d’une certification ISO 13485 atteste de l’existence d’un système de management de la qualité conforme aux exigences applicables aux dispositifs médicaux. Elle ne garantit pas à elle seule la performance clinique, mais constitue un indicateur de maturité organisationnelle et de maîtrise du cycle de vie du dispositif (gestion des risques, surveillance post-marché, amélioration continue).
Ainsi, dans un appel d’offres, le marquage CE IIa doit être analysé non comme une case à cocher, mais comme un point de départ pour interroger la solidité scientifique et réglementaire réelle du dispositif.
4. L’algorithme d’alerte est-il validé scientifiquement ?
Dans un appel d’offres télésurveillance insuffisance cardiaque, la conception de l’algorithme d’alerte est un élément déterminant. Toutes les solutions ne reposent pas sur la même logique clinique.
Approche mono-paramétrique : simplicité apparente, limites opérationnelles
Les systèmes dits de “première génération” déclenchent une alerte dès qu’un paramètre isolé (souvent le poids) dépasse un seuil prédéfini.
Chaque variable est analysée indépendamment. Cette approche peut conduire à :
-
une production d’alertes non pertinentes dès l’apparition d’un seul symptôme,
-
un volume élevé d’alertes nécessitant un filtrage manuel,
-
une charge organisationnelle supplémentaire pour les équipes,
-
un risque médico-légal si le filtrage est réalisé par des intervenants extérieurs sans accès complet au dossier clinique.
Les coûts et le temps liés au tri des alertes peuvent alors freiner la montée en charge du programme.
Approche multi-paramétrique : hiérarchisation clinique du risque
Les systèmes de “seconde génération” reposent sur un score combinant plusieurs paramètres pondérés (poids, dyspnée, œdèmes, fatigue, etc.). L’objectif n’est pas de détecter un symptôme isolé, mais d’évaluer un niveau de probabilité de décompensation cardiaque. Cette structuration permet :
-
de limiter les alertes non pertinentes,
-
de hiérarchiser le niveau de risque,
-
de soutenir la décision clinique plutôt que de la remplacer.
Un algorithme multi-paramétrique pertinent doit démontrer :
-
la base scientifique des pondérations utilisées,
-
des indicateurs statistiques publiés (sensibilité, spécificité, valeur prédictive négative),
-
une validation en conditions réelles d’utilisation.
À titre illustratif, une publication en vie réelle (Jourdain et al., 2023) rapporte une valeur prédictive négative de 99,43 % à 7 jours pour un score en zone verte, ce qui signifie qu’en l’absence d’alerte, la probabilité d’hospitalisation pour insuffisance cardiaque est très faible. Ce type d’indicateur est essentiel pour sécuriser l’organisation des soins.
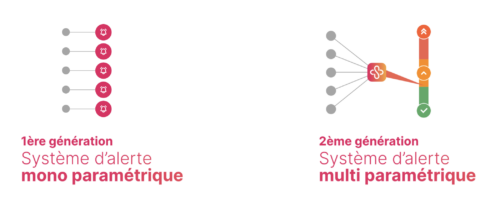
Intérêts et bénéfices d’un algorithme de télésurveillance multi paramétrique vs. mono paramétrique (Source)
Implications réglementaires des algorithmes paramétrables
La question de la paramétrabilité des seuils d’alerte ne doit pas être analysée uniquement sous l’angle opérationnel. Dans le cadre du règlement (UE) 2017/745 relatif aux dispositifs médicaux, un algorithme influençant la décision clinique fait partie intégrante du dispositif médical et de sa revendication de performance.
Toute modification des seuils, des règles de pondération ou de la logique de calcul susceptible d’impacter la performance clinique peut constituer une modification substantielle du dispositif. Elle peut alors nécessiter une mise à jour du dossier technique, une nouvelle évaluation clinique, voire une notification à l’organisme notifié.
Le marquage CE (généralement classe IIa pour les dispositifs de télésurveillance en insuffisance cardiaque) ne suffit pas à apprécier la solidité clinique d’un algorithme. Il convient d’examiner :
-
la revendication exacte associée au marquage CE (revendication technique ou revendication de performance clinique),
-
les données cliniques ayant soutenu cette revendication,
-
la cohérence entre les performances publiées et l’usage réel du dispositif,
-
l’existence d’un système qualité certifié (ISO 13485) encadrant la gestion des modifications algorithmiques.
Un dispositif permettant une personnalisation locale des seuils doit pouvoir démontrer que ces adaptations restent couvertes par sa validation réglementaire et sa revendication initiale. À défaut, un décalage peut apparaître entre l’usage réel et le périmètre validé, avec des implications médico-légales pour l’établissement.
Dans un appel d’offres télésurveillance insuffisance cardiaque, l’analyse réglementaire de l’algorithme est donc indissociable de son évaluation clinique.
Conclusion
Dans un appel d’offres télésurveillance insuffisance cardiaque, l’algorithme d’alerte doit être analysé comme un élément clinique structurant, et non comme une simple fonctionnalité technique. La distinction entre approche mono-paramétrique et multi-paramétrique permet d’évaluer la maturité réelle du dispositif : capacité à hiérarchiser le risque, à limiter les alertes inutiles et à sécuriser l’absence d’alerte.
Au-delà des performances annoncées, l’acheteur doit s’assurer de trois points essentiels :
-
la solidité scientifique des pondérations
-
la publication d’indicateurs en vie réelle
-
et la conformité réglementaire des évolutions (MDR 2017/745, marquage CE, ISO 13485).
C’est cette cohérence entre logique clinique, validation scientifique et encadrement réglementaire qui conditionne la sécurité et la pérennité d’un programme de télésurveillance.
5. La solution est-elle adaptée aux patients âgés et en situation d’illectronisme ?
Alors que l’âge moyen de survenue de l’insuffisance cardiaque est de 73,5 ans (Épidémiologie de l’insuffisance cardiaque par F. Delahaye, G. de Gevigney), 62 % des plus de 75 ans ne maîtrisent pas les outils numériques selon l’INSEE (2023), . L’insuffisance cardiaque touche majoritairement cette tranche d’âge.
Un appel d’offres en télésurveillance insuffisance cardiaque doit interroger :
-
l’existence de modalités alternatives (téléphone, accompagnement humain),
-
la simplicité d’inclusion,
-
l’absence d’obligation d’équipements complexes.
6. L’accompagnement thérapeutique est-il structuré conformément au cadre réglementaire ?
Le droit commun impose un accompagnement thérapeutique formalisé. La Cochrane Review (2017) montre que l’éducation thérapeutique réduit les hospitalisations. Il convient d’examiner :
-
la formation des intervenants,
-
la traçabilité des séances,
-
la structuration du programme.
7. La solution facilite-t-elle la coordination du parcours de soins ?
La HAS rappelle que l’efficacité dépend de l’intégration dans le parcours global (HAS, Avis DMN IC, 2023). Un dispositif mature doit permettre :
-
le chargement sécurisé des documents médicaux,
-
la coordination des analyses biologiques,
-
le suivi vaccinal,
-
la centralisation des données cliniques.
La télésurveillance ne doit pas être un outil isolé, mais un maillon du parcours.
8. Le dispositif permet-il un pilotage clair et conforme de l’activité ?
Le cadre réglementaire impose :
-
la lecture bihebdomadaire des alertes,
-
la traçabilité des transmissions,
-
le suivi de l’utilisation effective.
Il est pertinent d’évaluer :
-
la visualisation de la file active,
-
la hiérarchisation des patients par niveau de risque,
-
l’aide à la facturation conforme aux exigences du droit commun.
9. La solution bénéficie-t-elle d’une reconnaissance réglementaire spécifique ?
Au-delà de la ligne générique, certaines solutions ont été reconnues individuellement en “nom de marque” par les autorités sanitaires. Cette reconnaissance signifie que les performances propres du dispositif ont été évaluées distinctement et jugées différenciantes.
Dans un appel d’offres télésurveillance insuffisance cardiaque, il est pertinent d’examiner :
-
le statut réglementaire exact,
-
le niveau tarifaire attribué,
-
les données scientifiques ayant fondé cette reconnaissance.
10. Le modèle économique est-il sécurisé à l’horizon de la réévaluation 2026 ?
La ligne générique actuelle fera l’objet d’une réévaluation au 1er juillet 2026. Cette réévaluation prendra en compte :
-
les données cliniques disponibles,
-
les données en vie réelle,
-
l’impact organisationnel,
-
l’efficience médico-économique.
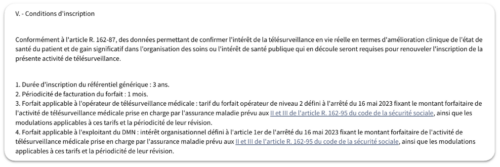
Extrait du Journal Officiel faisant état de la date de fin d’inscription du référentiel générique de la télésurveillance de l’insuffisance cardiaque au 1er juillet 2026
En l’absence de preuves scientifiques publiées démontrant un bénéfice tangible, le risque est :
-
une révision du niveau de remboursement,
-
une fragilisation des solutions insuffisamment documentées.
Ainsi, dans un appel d’offres, la soutenabilité économique est directement liée à la solidité scientifique du dispositif.
Conclusion : structurer un appel d’offres télésurveillance insuffisance cardiaque sur des critères objectifs
Un appel d’offres en télésurveillance insuffisance cardiaque engage durablement un établissement. Il doit s’appuyer sur :
-
des preuves cliniques publiées,
-
une conformité réglementaire opérationnelle,
-
une validation algorithmique documentée,
-
une accessibilité aux patients âgés,
-
une intégration réelle dans le parcours de soins,
-
une sécurisation économique à moyen terme.
Ces critères permettent une comparaison objective et sécurisent la décision.
Télécharger la grille d’évaluation pour votre appel d’offres télésurveillance insuffisance cardiaque
Nous mettons à disposition une grille d’analyse prête à intégrer dans votre DCE, incluant :
-
exigences réglementaires issues du JO du 24 juin 2023,
-
critères cliniques ESC,
-
critères organisationnels,
-
points de vigilance liés à la réévaluation 2026.
👉 Télécharger la grille d’évaluation (PDF)
Foire aux questions – Appel d’offres télésurveillance insuffisance cardiaque
Qu’est-ce qu’un appel d’offres télésurveillance insuffisance cardiaque ?
Un appel d’offres télésurveillance insuffisance cardiaque est un processus structuré permettant de sélectionner une solution conforme au droit commun, intégrant des preuves cliniques publiées et des garanties réglementaires.
Quels critères réglementaires doivent être vérifiés ?
Le dispositif doit respecter l’arrêté du 22 juin 2023, intégrer un questionnaire symptomatique structuré et assurer la traçabilité des alertes.
Pourquoi vérifier le marquage CE et la certification ISO 13485 ?
Le marquage CE doit préciser la revendication clinique associée. La certification ISO 13485 garantit un système qualité conforme aux exigences européennes des dispositifs médicaux.
Comment anticiper la réévaluation de la ligne générique en 2026 ?
Il est indispensable de choisir une solution disposant de preuves cliniques publiées afin de sécuriser le maintien du remboursement.

